Qu'est-ce que Foscan ?
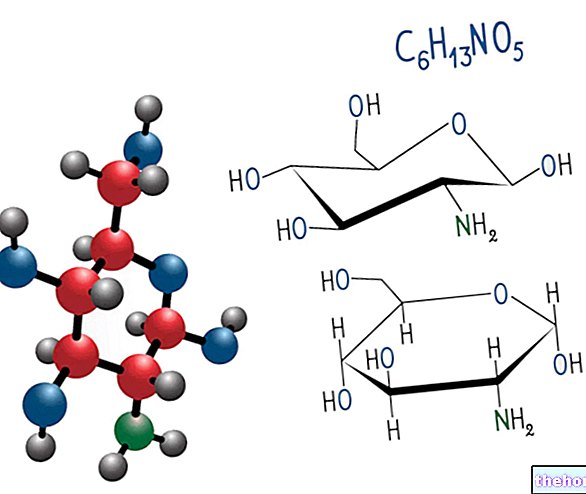
Foscan est une solution injectable qui contient le principe actif témoporfine (1 ou 4 mg/ml).
A quoi sert Foscan ?
Foscan est utilisé pour soulager les symptômes du carcinome épidermoïde de stade avancé de la tête et du cou (un type de cancer qui prend naissance dans les cellules qui tapissent la bouche, le nez, la gorge ou l'oreille). plus efficaces et ne sont pas adaptés à la radiothérapie (radiothérapie), à la chirurgie ou à la chimiothérapie systémique (médicaments utilisés dans le traitement du cancer ; « systémique » signifie qu'ils sont destinés à agir sur l'ensemble du corps).
Le médicament ne peut être obtenu que sur ordonnance.
Comment Foscan est-il utilisé ?
Foscan ne doit être administré que dans un centre spécialisé dans le traitement du cancer, où une équipe peut évaluer le traitement du patient sous la supervision d'un médecin expérimenté en thérapie photodynamique (traitement utilisant l'action de la lumière). Le traitement avec Foscan est un processus en deux étapes : le médicament est d'abord administré puis activé à l'aide d'un laser. Le médicament est administré par une canule intraveineuse permanente (un tube mince inséré de façon permanente dans une veine) en une seule injection lente sur une période d'au moins six minutes. La dose est de 0,15 mg par kilogramme de poids corporel. Quatre jours plus tard, toute la zone touchée par la tumeur doit être éclairée, jusqu'à 0,5 cm au-delà de la marge environnante, avec une lumière générée par une source laser à une longueur d'onde spécifique pendant environ 3 minutes et 20 secondes à l'aide d'un câble à fibre optique. Chaque zone du tissu tumoral ne doit être éclairée qu'une seule fois pendant chaque traitement.Pendant le traitement, les autres zones du corps doivent être protégées de la lumière, de sorte que le médicament ne soit activé que sur la tumeur. Si un deuxième cycle est nécessaire, il doit être effectué avec un intervalle minimum de quatre semaines.
Comment fonctionne Foscan ?
Le principe actif contenu dans Foscan, la témoporfine, est un agent photosensibilisant (substance qui change lorsqu'elle est exposée à la lumière). Après l'injection de Foscan, la témoporfine est distribuée dans tout le corps, y compris dans la masse tumorale. Lorsqu'il est éclairé avec la lumière laser à un
étant donné la longueur d'onde, la témoporfine est activée et réagit avec l'oxygène présent dans les cellules, créant un type d'oxygène hautement réactif et toxique. Il tue les cellules en réagissant avec leurs composants (protéines et ADN) et en les détruisant. En limitant l'éclairage à la tumeur, seules les cellules tumorales sont endommagées, sans affecter les autres parties du corps.
Comment Foscan a-t-il été étudié ?
Foscan a fait l'objet de quatre études principales portant sur un total de 409 patients atteints d'un cancer de la tête ou du cou. Les trois premières études visaient à examiner si le cancer avait été guéri après jusqu'à trois cycles de traitement avec Foscan chez un total de 189 patients. La quatrième étude s'est concentrée sur la réduction des symptômes chez 220 patients atteints d'un cancer avancé de la tête et du cou qui ne pouvaient pas subir de chirurgie ou de radiothérapie. Dans toutes les études, la réponse au traitement a été évaluée entre la 12e et la 16e semaine suivant le dernier cycle avec Foscan ; cependant, Foscan n'a été comparé à aucun autre médicament.
Quel bénéfice Foscan a-t-il démontré au cours des études ?
Les résultats des trois premières études n'ont pas semblé suffisants pour corroborer l'efficacité de Foscan dans l'éradication des cancers de la tête et du cou. En revanche, dans l'étude qui a évalué l'amélioration des symptômes chez les patients atteints d'un cancer de la tête et du cou à un stade avancé, 28 patients (22%) sur les 128 sujets observés ont montré une amélioration significative des symptômes les plus gênants. Une réduction de la taille de la tumeur a également été observée chez environ un quart des patients impliqués dans cette étude.
Quel est le risque associé à Foscan ?
Les effets indésirables les plus fréquents avec Foscan (observés chez plus de 1 patient sur 10) sont des douleurs au site d'injection, dans la tumeur ou au visage, des saignements, des cicatrices, une nécrose de la bouche (mort de cellules ou de tissus dans la bouche) , dysphagie (difficulté à avaler), œdème du visage (gonflement) et constipation.Pour la liste complète des effets indésirables rapportés avec Foscan, voir la notice.
Foscan ne doit pas être utilisé chez les personnes pouvant présenter une hypersensibilité (allergie) à la témoporfine ou à l'un des composants. Foscan ne doit pas être utilisé chez les patients atteints de porphyrie (incapacité à métaboliser les porphyrines), d'autres maladies exacerbées par la lumière, d'allergie aux porphyrines ou de tumeurs qui se propagent à un vaisseau sanguin ou sont proches du site d'illumination. Foscan ne doit pas non plus être administré aux patients devant subir une intervention chirurgicale dans les 30 jours, aux patients atteints d'une maladie oculaire nécessitant une évaluation à la "lampe à fente" (outil utilisé par les ophtalmologistes pour regarder à l'intérieur de l'œil). les 30 prochains jours ou aux patients qui sont déjà traités avec un autre médicament qui augmente la sensibilité à la lumière.
Pendant les six mois suivant l'injection de Foscan, les patients doivent éviter de s'exposer à une lumière vive pour éviter le risque de brûlures cutanées. Veuillez vous référer à la notice pour plus de détails.
Pourquoi Foscan a-t-il été approuvé ?
Le comité des médicaments à usage humain (CHMP) a conclu que les effets de Foscan dans le soulagement des symptômes associés au cancer avancé de la tête et du cou étaient remarquables. Par conséquent, le comité a décidé que les bénéfices de Foscan sont supérieurs à ses risques pour le traitement palliatif des patients. atteints d'un carcinome épidermoïde avancé de la tête et du cou qui ont échoué aux traitements antérieurs et ne sont pas adaptés à la radiothérapie, la chirurgie ou la chimiothérapie systémique. Le comité a recommandé la libération de l'autorisation de mise sur le marché de Foscan.
Foscan a été initialement autorisé dans des "circonstances exceptionnelles" car, du fait de la rareté de la maladie et pour des raisons scientifiques, les informations étaient rares au moment de l'autorisation. La société ayant fourni les informations complémentaires demandées, la restriction des "circonstances exceptionnelles" " a été retiré le 21 mai 2008.
Autres informations sur Foscan :
Le 24 octobre 2001, la Commission européenne a délivré une « autorisation de mise sur le marché » pour Foscan, valable dans toute l'Union européenne.
le commerce a été renouvelé le 24 octobre 2006. Le titulaire de l'autorisation de mise sur le marché est la société Biolitec Pharma ltd.
Pour la version complète de l'EPAR Foscan, cliquez ici.
Dernière mise à jour de ce résumé : 05-2008
Les informations sur Foscan - témoporfin publiées sur cette page peuvent être obsolètes ou incomplètes. Pour une utilisation correcte de ces informations, consultez la page Avis de non-responsabilité et informations utiles.