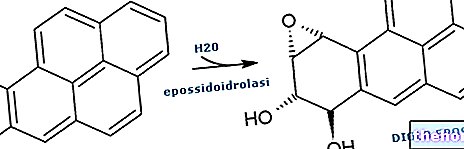
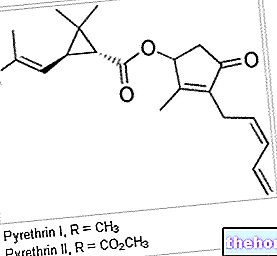
La cancérogenèse est étudiée avec divers tests toxicologiques standardisés. Une première partie de ces tests est réalisée in vitro, et - s'ils sont positifs - on procède à une expérimentation in vivo. Cette approche expérimentale étape par étape s'appelle DECISION POINT APPROACH, une séquence d'essais qui s'arrêtent à la fin de chaque essai pour décider de la manière de procéder. Il y a cinq étapes :
PHASE A : structure et caractéristiques du composé cancérigène ;
PHASEB : dans cette phase de test in vitro à court terme, des cellules de mammifères sont utilisées. Les cellules les plus couramment utilisées sont les hépatocytes, car l'étendue de la réparation des dommages que l'hépatocyte développe en fonction de la gravité des dommages causés par la substance est étudiée. En un mot, nous déterminons non pas les dommages en soi, mais quelle quantité du système de réparation a été activée par la cellule hépatique.
Le mode opératoire mis en œuvre consiste à former 3 cultures d'hépatocytes. Dans la première culture les hépatocytes sont sains, dans la seconde ils sont traités avec la substance à tester et enfin dans la troisième ils sont traités avec une substance témoin qui est certainement cancérigène.Ces trois cultures contiennent une base pyrimidique radioactive, qui est la thymidine tritiée, qui joue le rôle de marqueur.
Si le composé examiné provoque une mutation de l'ADN, la cellule répond à ce problème en activant les systèmes de réparation. Le morceau d'ADN qui a subi la mutation est coupé et grâce à l'action de l'ADNpolymérase le morceau manquant est remplacé par un nouveau.Pour la correction, l'ADNpolymérase utilise les nouvelles bases, dont la thymidine tritiée.Une base radioactive est incorporée. L'analyse de la radioactivité détermine le niveau de mutation dans les cellules traitées : plus la radioactivité est élevée, plus les mutations de l'ADN sont importantes.
Toujours en phase B, des tests sont également effectués sur des bactéries, pour pouvoir étudier s'il existe des mutations inverses. Les bactéries utilisées sont des salmonelles déjà porteuses de mutations. La mutation concerne la synthèse de l'histidine, les salmonelles sont donc incapables de se développer sans histidine. Ces colonies bactériennes sont en partie prises pour être traitées avec la substance d'essai, en partie pour le contrôle négatif et en partie pour le contrôle positif, puis testées avec un cancérogène connu. Si cette substance d'essai est génotoxique indirecte, des enzymes métabolisantes doivent être introduites dans le milieu de culture. A ce stade, il y a 3 cultures qui seront ensemencées et cultivées dans des boîtes de Pétri (il n'y a pas d'histidine dans le milieu de culture).S'il n'y a pas eu de mutations du cancérogène à tester, en théorie il ne devrait y en avoir aucune sur les plaques S'il y a eu une action mutagène du cancérogène, il peut avoir modifié la première mutation et créé une deuxième mutation capable de faire croître la bactérie sur le milieu de culture sans histidine.Dans ce cas, la deuxième mutation qu'il modifie la première mutation et prend le nom de RETROMUTATION Enfin, si une croissance importante se produit dans la piasta petri, le cancérogène est direct.
Toujours avec un test in vitro, il est possible de déterminer l'intégrité chromosomique.Ce test est toujours réalisé sur des cellules de mammifères et sert à tester des substances toxiques capables de provoquer des mutations sur certaines enzymes responsables de la biosynthèse de l'ADN.La substance à tester est soumis à une analyse in vitro Pour pouvoir déterminer si la substance examinée affecte l'intégrité et le nombre de chromosomes présents, le test du micronoyau est utilisé. Les micronoyaux sont des vésicules formées avec une partie de la chromatine à l'intérieur. La chromatine incorporée dans ces micronoyaux peut être soit des chromosomes entiers, soit des fragments de chromosomes. Les micronoyaux sont formés par la mauvaise division cellulaire donnant naissance à des cellules filles dont le matériel génétique n'est pas également égal. Le résultat de ce test sera la détermination de substances qui sont définies comme des poisons clastogènes et des poisons du fuseau. les micronoyaux qui à l'intérieur sont présents des chromosomes entiers.
Si la substance examinée induit une génotoxicité dans un ou plusieurs tests, celle-ci est définie comme hautement suspecte, elle passe donc directement en phase D. Si, en revanche, la substance testée ne produit aucun effet génotoxique, elle passe en phase d'étude C parce qu'il peut être un promoteur.
FASEC : dans cette phase, des tests in vitro et in vivo peuvent être effectués.
Pour les tests in vitro, il a pu être démontré la possibilité pour la substance promotrice de rompre les jonctions lacunaires entre les cellules normales et les cellules tumorales, avec pour conséquence le passage de substances entre les deux cellules.
Un test in vivo est l'induction de tumeurs cutanées chez la souris. La substance à tester est appliquée deux ou trois fois par semaine sur la peau de la souris. Dans les 2/3 mois si cette substance est un promoteur, il peut y avoir des formations de papillome. Chez la souris, deux données principales sont considérées : le nombre de souris atteintes de papillomes et le nombre de papillomes présents sur chaque animal. Si la substance agit comme un promoteur et développe une tumeur chez la souris traitée, cela signifie qu'il s'agit bien d'une substance à effet promoteur.
Une fois ces tests terminés, nous passons à des tests in vivo de longue durée.
FASED : dans cette phase, tous les composés qui s'avèrent mutagènes et tous les composés qui ne s'avèrent pas mutagènes sont testés. Les tests qui peuvent être effectués sont différents, dont certains sont des tests réalisés sur le foie, sur le poumon et enfin sur le sein.
Le test hépatique démontre la formation non pas d'une tumeur nouvellement formée, mais d'un foyer néoplasique, donc quelque chose qui se prépare à devenir une tumeur. Les cellules de ce foyer sont déjà des cellules atypiques, elles ont donc subi une mutation et se préparent à devenir des cellules néoplasiques. Après un certain temps, grâce à l'examen d'autopsie, la formation de foyers pré-néoplasiques est déterminée, en calculant le nombre et l'étendue de ces formations pré-néoplasiques.
Le test pulmonaire permet la détermination d'un adénome, qui est une « anomalie des cellules du tissu pulmonaire. Dans ce cas également le tissu pulmonaire du rat est examiné après un temps assez long (des mois) (ces adénomes sont facilement identifiables car sont des nodules blanchâtres sur l'épithélium pulmonaire).
Le test mammaire permet la détermination des tumeurs dans le tissu glandulaire. Le nombre d'adénomes formés et le nombre d'animaux présentant des adénomes sont toujours évalués.
Si ces tests donnent des résultats positifs, la substance d'essai est véritablement cancérigène. À ce stade, nous passons à la réalisation de tests coûteux avec des temps d'exécution très longs.
PHASEE : dans cette phase un nombre variable d'animaux, de 20 à 50, sont soumis à des tests de longue durée, tests très coûteux et longs à obtenir certains résultats ; on parle d'environ 1/8 de la vie de l'animal.Il est possible qu'au cours de ces tests certains animaux meurent, mais ils sont toujours étudiés avec une autopsie et un examen de type histologique. Les animaux choisis sont toujours des rats et des souris et seuls 70 à 80 % survivent jusqu'à la fin des tests de longue durée. Les animaux utilisés sont juste sevrés, car plus ils sont jeunes, plus ils sont sensibles aux traitements. Pendant la période d'essai de longue durée, le chercheur est toujours épaulé par un mathématicien-statisticien, capable de prendre en compte l'ensemble des informations recueillies et de reproduire les différentes données.
Les doses testées sur les animaux partent de la dose maximale tolérée et de tous ses sous-multiples, et la réaction dose-réponse chez l'animal est évaluée.
L'administration doit toujours se rapprocher de la voie par laquelle l'homme peut entrer en contact avec la substance examinée, donc la voie orale, cutanée ou respiratoire, alors que si la cancérogénicité d'un médicament est testée, il est également utile de procéder à une administration intraveineuse.
Les groupes d'animaux testés sont au nombre de 4 (50 animaux pour chaque groupe) :
- Un groupe NAIF qui n'a pas de traitement ;
- Un groupe soigné avec le véhicule ;
- Un groupe traité avec la substance d'essai ;
- Un groupe traité avec un cancérigène connu.
Il est très important que le nombre d'animaux dans chaque groupe soit le plus égal possible.En effet, s'il y a trop de différence dans le nombre d'animaux, le test statistique peut s'avérer faux.
Les évaluations qui sont effectuées sont :
- Fréquence totale des tumeurs ;
- Fréquence de certaines tumeurs ;
- Fréquence des animaux avec plus d'un type de tumeur ;
- Nombre de cancers animaux.
A l'issue de toutes ces phases d'étude, la substance est classée dans un classement établi par le CIRC (Centre International de Recherche et de Développement sur le Cancer) et par l'Environmental Protection Agency (EPA).
Autres articles sur "Étude et évaluation de la cancérogenèse"
- Carcinogenèse
- Toxicité et toxicologie
- Toxicologie du cycle de reproduction et tératogenèse